编者按
创伤性脑损伤(TBI)是神经退行性疾病的主要环境风险因素,每年估计发生超过6000万例。最近的研究表明TBI与神经毒性蛋白tau、TDP-43和β淀粉样蛋白的病理性积聚有关,导致慢性创伤性脑病(CTE)、肌萎缩侧索硬化(ALS)、阿尔茨海默病和其他痴呆症等进行性神经退行性疾病。一次中度至重度的TBI会使患老年痴呆的风险增加4倍。
今天我们来分享一篇2024年4月4日由南加州大学凯克医学院Justin K. Ichida团队发表在Cell Stem Cell杂志(IF=23.9)上的一项最新研究——《KCNJ2 inhibition mitigates mechanical injury in a human brain organoid model of traumatic brain injury》,该研究开发了一种高强度超声平台来实施机械损伤,并利用脑类器官,揭示了神经元亚型在损伤易感性上的关键差异,并建立了一个监测不同人类遗传背景下损伤反应的方法。抑制KCNJ2可能有助于减轻脑损伤后早期神经元死亡。
文章题目
KCNJ2 inhibition mitigates mechanical injury in a human brain organoid model of traumatic brain injury
杂志:《Cell Stem Cell》(IF=23.9)
发表时间:2024年4月4日
作者:Justin K. Ichida团队
单位:南加州大学凯克医学院
01、皮层类器官损伤与TBI相关的标志物
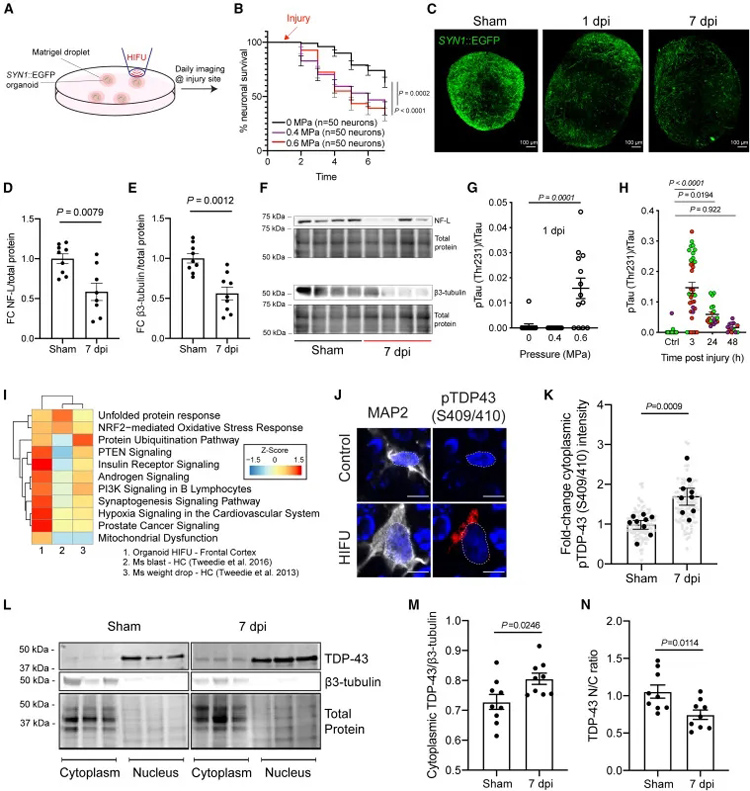
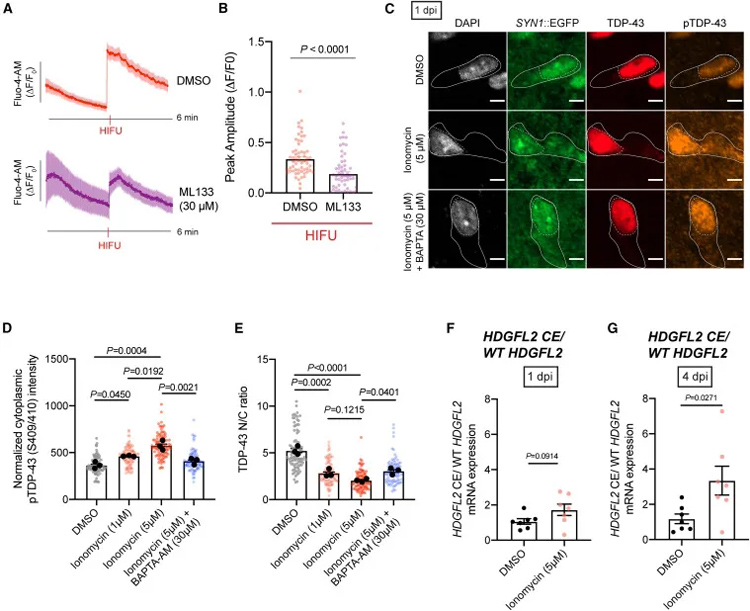
研究团队首先使用高强度聚焦超声波(HIFU)技术对诱导多能干细胞(iPSC)来源的脑类器官进行机械损伤,通过慢病毒转染(SYN1::eGFP)标记兴奋性神经元,成功模拟了TBI的关键病理特征,包括神经元死亡、tau蛋白磷酸化和TDP-43核输出。
在对TBI的生物标志物进行检测后,研究人员发现在受伤的皮层类器官中,磷酸化tau蛋白水平增加、神经元死亡,神经元的胞质中显著聚集磷酸化的TDP-43。RNA测序结果和活细胞成像也验证了,类器官出现与TBI一致的变化特征。
这些结果表明,通过HIFU损伤皮层皮层类器官,可以模拟TBI相关的生物标志物和疾病机制。
02、深层神经元损伤后表现出增强的TDP-43功能障碍
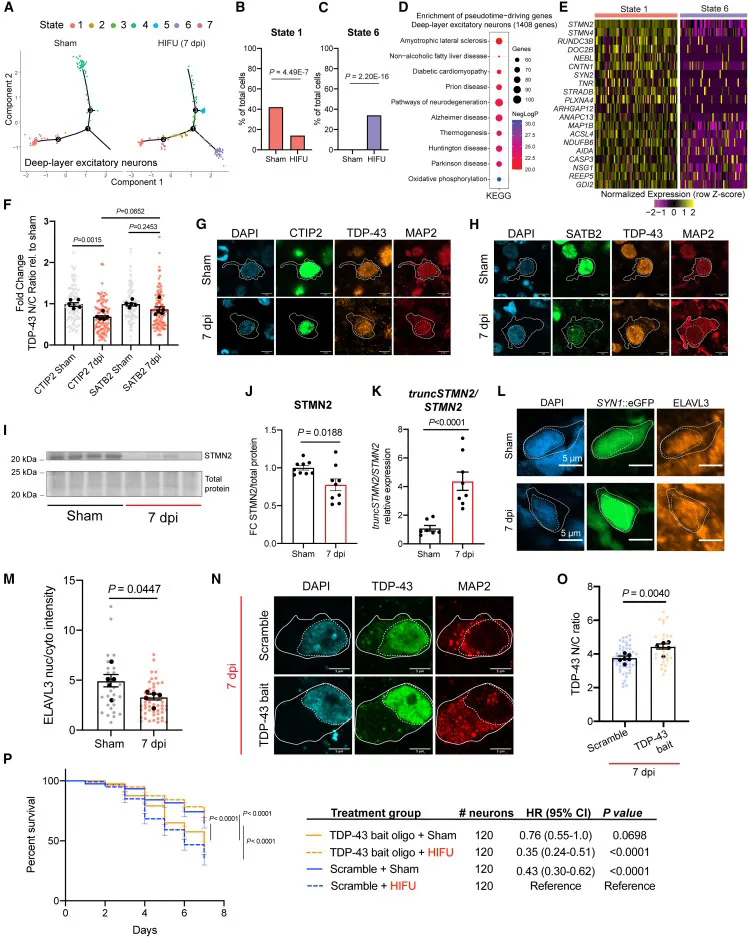
随后,研究人员对2,530个类器官细胞进行单细胞RNA测序发现,未接受损伤和深层损伤的神经元间差异表达的基因富集多种神经退行性疾病,最显著的是肌萎缩性侧索硬化症。
利用人类iPSC脑类器官模型研究表明,在深层神经元中发生的TDP-43功能障碍,是神经元死亡的主要驱动因素,并且在肌萎缩侧索硬化症(ALS)和额颞叶痴呆(FTD)神经元中更为明显。TDP-43功能丧失,导致深层兴奋性神经元中许多潜在的TDP-43靶基因表达下调,这可能是机械损伤后TDP-43功能丧失的标志。
进一步分析发现,受损的深层兴奋性神经元中,许多TDP-43靶向的基因出现明显下调,提示机械损伤破坏了TDP-43的功能,随后的免疫染色、mRNA以及蛋白结果验证了这一点。在没有损伤的情况下,用诱饵寡核苷酸治疗诱导神经元死亡。该诱饵基于 TDP-43 的充分表征的高亲和力核酸序列。在没有损伤且细胞质TDP-43 升高的情况下,高浓度的这些寡核苷酸可能会进入细胞核,在那里它们可能会竞争性取代TDP-43偏离其正常目标,通过新生转录的剪接失调导致靶向毒性。
结果显示,这一操作显著提升了损伤后神经元TDP-43的核质比。这说明TDP-43功能障碍在损伤诱导的神经元死亡中起着重要作用,且其倾向于影响深层神经元。
03、抑制KCNJ2可减轻HIFU诱导的神经元死亡
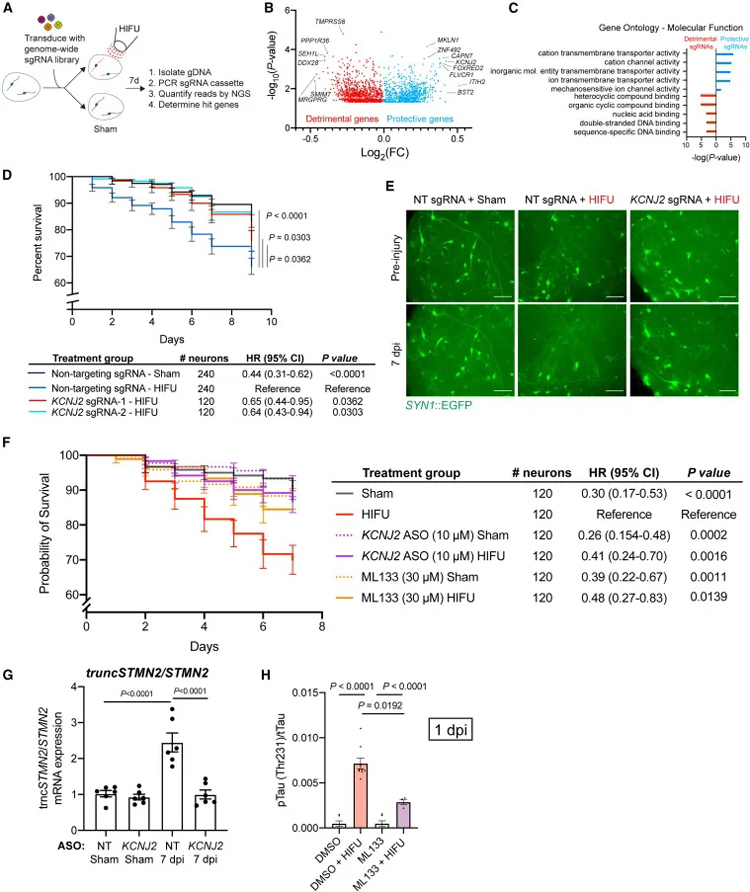
利用全基因组CRISPR干扰筛选,作者鉴定了最佳的靶点KCNJ2。KCNJ2的遗传敲除和小分子抑制均显示出维持受损皮层类器官中神经元存活的效果。研究表明,抑制KCNJ2可以减轻HIFU引起的神经元死亡,降低p-Tau与总Tau比率。
KCNJ2通过调节Ca2+通量导致TDP-43功能障碍,而KCNJ2的抑制可以减轻这些过程,显示了其在神经保护中的潜在作用。
对其作为治疗的潜力至关重要的是,损伤后 1 小时对KCNJ2的小分子抑制足以改善神经元存活。这与当前药物干预措施的治疗窗一致,例如巴比妥类药物,通常在人类TBI后 1-2 小时内给药。KCNJ2抑制也可被视为对TBI急性风险较高的个体的预防性治疗。
此外,通过在小鼠模型中进行控制皮层撞击(CCI)实验,研究人员验证了KCNJ2抑制对TBI的保护作用。
研究发现,在小鼠脑损伤模型中,使用Kcnj2 反义寡核苷酸治疗可显著减少神经元TDP-43核质比和细胞质TDP-43在损伤部位的聚集。Kcnj2 反义寡核苷酸治疗还降低了细胞死亡和星形胶质增多,减少了细胞质中的磷化TDP-43水平。
Kcnj2 反义寡核苷酸还减少了损伤部位附近的细胞死亡和星形胶质增多。研究显示,Kcnj2抑制显著减少了脑损伤后的TDP-43损伤和退行性反应。
这不仅揭示了TBI后大脑病理学的分子机制,而且还为开发新的治疗策略提供了潜在的靶点——KCNJ2,这对于未来治疗TBI及其相关神经退行性疾病具有重要意义。通过深入了解TBI如何与神经退行性疾病相互关联,这项工作为未来的神经保护和修复策略提供了重要的科学基础。
04、编者点评
总体而言,这篇文章介绍了一个用于发现和验证机械损伤修饰剂的人体类器官平台。该损伤模型旨在弥合传统体外系统和复杂高等生物之间的差距,提供可扩展且遗传灵活的系统,以确定TBI急性和慢性影响的潜在疾病机制和治疗方法。
研究人员发现 TDP-43 功能障碍是机械损伤后神经元死亡的关键驱动因素,并确定了深层兴奋性神经元对 TDP-43 功能障碍的内在脆弱性。最后,在已建立的TBI小鼠模型以及携带导致ALS/FTD的突变的健康和患病类器官中,KCNJ2抑制可有效减轻损伤诱发的疾病过程,部分是通过损伤后胞质 Ca2+ 的神经保护性减少。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”四位一体的综合技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型及脑类器官、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
参考文献
SKCNJ2 inhibition mitigates mechanical injury in a human brain organoid model of traumatic brain injury: Cell Stem Cell
